Vous êtes ici
Thématique:
Masses thoraciques de l’enfant
![]()
C. Thumerelle1, S. Lejeune1, H. Ducou Le Pointe2
1CHU Lille, Service de pneumo-allergologie pédiatrique, Hôpital Jeanne-de-Flandre, Université de Lille, F-59000 Lille, France2Service de radiologie, CHU Armand-Trousseau (AP-HP), Sorbonne Université, Paris, France
*Auteur correspondant - Adresse e-mail : caroline.thumerelle@chru-lille.fr (C. Thumerelle). Cliquez sur l'image pour l'agrandir.
| Article validé par : | |
|
SFCE (Société Française de lutte contre le Cancer et les leucémies de l’Enfant et de l’Adolescent) |
|
|
SFCP (Société Française de Chirurgie Pédiatrique) |
|
|
SFIPP (Société Francophone d’Imagerie Pédiatrique et Prénatale) |
|
|
SP2A (Société Pédiatrique de Pneumologie et Allergologie) |
|
| Remerciements aux relecteurs : | |
|
J.-H. Dalle V. Gandemer (SFCE) O. Abbo E. Habomimana E. Hervieux N. Khen Dunlop F. Lavrand C. Piolat R. Sfeir (Comité Thorax et Groupe Cancer de la SFCP) H. Brisse (SFIPP) L. Giovanni-Chami C. Schweitzer (SP2A |
|
Introduction
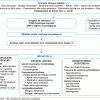
Les masses thoraciques de l’enfant peuvent correspondre à de multiples causes : malformatives, infectieuses, tumorales bénignes ou malignes.
(1) Le mode de révélation clinique de ces masses correspond à des contextes très variables selon l’étiologie, avec le plus souvent une suspicion de masse sur une radiographie de thorax. Les tumeurs malignes sont associées à des tableaux cliniques plus manifestes liés à l’envahissement et aux compressions exercées par la masse (possibilité de syndrome cave supérieur, d’obstruction des voies aériennes avec bruits respiratoires, de signes neurologiques de compression médullaire), et sont parfois associées à une altération de l’état général.
Conduite à tenir face à une masse thoracique
(2) L’imagerie de référence est avant tout la tomodensitométrie (TDM) thoracique avec injection. Elle permet de confirmer la présence d’une masse, de préciser sa localisation et sa nature.
(3) Éliminer les « pseudo-masses » est la première étape diagnostique. L’échographie thoracique, notamment chez le nourrisson, peut être un bon examen pour l’analyse du médiastin antérieur et postérieur et son indication peut être discutée avec le radiologue. Elle permettra d’éviter une TDM dans les situations évocatrices de thymus ectopique ou proéminent, de goitre intrathoracique, et de certaines anomalies de la paroi thoracique. L’échographie permet également un débrouillage en cas d’hémithorax blanc radiographique en distinguant les épanchements pleuraux liquidiens des masses tissulaires.
(4) L’analyse de la masse selon sa localisation (médiastin, paroi thoracique, poumon), ses rapports anatomiques et sa composition permet de poursuivre l’approche étiologique.
(5) Les masses médiastinales sont d’origine étiologique différente selon la zone concernée avec une séparation en trois compartiments (Figure 1) : prévasculaire (antérieur), viscéral (moyen) et paravertébral (postérieur).
Le médiastin prévasculaire comprend le thymus, de la graisse et des ganglions lymphatiques. Les principales anomalies sont les malformations lymphatiques (lymphangiomes kystiques), les lymphomes, les tératomes matures ou non, les adénopathies, et les tumeurs germinales malignes. En dehors des lymphomes, les tumeurs thymiques sont très rares en pédiatrie.
Le médiastin viscéral comprend des structures vasculaires (coeur, aorte, veine cave supérieure, canal thoracique) et non vasculaires (trachée, oesophage, ganglions lymphatiques). L’atteinte la plus fréquente de ce compartiment concerne le système lymphatique avec les adénopathies d’origine lymphomateuse, infectieuse (tuberculose) ou inflammatoire (sarcoïdose), les lymphangiomes, les kystes malformatifs de l’intestin primitif (kyste bronchogénique et duplication oesophagienne) ou pleuropéricardiques.
Le médiastin paravertébral comprend surtout le rachis et le tissu mou para-rachidien. Les tumeurs sont le plus souvent neuroblastiques chez l’enfant avec le neuroblastome et le ganglioneuroblastome, surtout avant l’âge de 5 ans. L’imagerie par résonance magnétique (IRM) thoracique est de première intention en cas de symptômes neurologiques, et préférentielle dans la caractérisation de ces tumeurs et l’étude de leur extension locorégionale. Le diagnostic sera complété par une scintigraphie à la méta-iodo-benzyl-guanidine (MIBG) et un dosage des catécholamines urinaires. Après l’âge de 7 ans, les tumeurs neuroblastiques les plus fréquentes sont les ganglioneuromes matures, bénins, dont le diagnostic sera confirmé en anatomopathologie.
(6) Les masses d’origine pariétale ont une origine musculo-squelettique mais peuvent s’étendre dans un hémithorax complet. L’IRM thoracique complète le plus souvent la TDM dans l’évaluation de la tumeur et de ses rapports.
Parmi les tumeurs d’origine osseuse, la famille des sarcomes d’Ewing (comprenant les tumeurs d’Askin, les Ewing typiques et atypiques, et les tumeurs primitives neuro-ectodermiques périphériques) est la plus représentée concernant surtout les enfants âgés de plus de 12 ans. Une analyse fine de l’os en TDM permet de suspecter l’atteinte costale primitive ou plus rarement extraosseuse postérieure.
Les rhabdomyosarcomes (RMS) sont les tumeurs malignes des tissus mous les plus fréquentes chez l’enfant. Tout le thorax peut être concerné avec le plus souvent une extension à partir de la paroi thoracique, mais un point de départ médiastinal, pulmonaire, diaphragmatique ou cardiaque est possible. Il s’agit de tumeurs solides, parfois nécrotiques sans aspect radiologique distinct.
Les tumeurs bénignes de la paroi thoracique peuvent être asymptomatiques, perçues à la palpation, découvertes sur une complication locale (fracture, épanchement pleural) ou à l’occasion d’un examen d’imagerie. Pour les tumeurs costales, les ostéochondromes sont les plus fréquents ; les granulomes éosinophiles sont associés aux histiocytoses langerhansiennes et ont souvent un aspect lytique. De multiples autres tumeurs sont possibles : ostéome, ostéome ostéoïde, neurofibrome, dysplasie fibreuse, etc. Une tumeur particulière est l’hamartome mésenchymateux costal qui concerne surtout les nourrissons, et qui a un aspect hétérogène associant une atteinte osseuse soufflante et une masse des tissus mous avec des zones kystiques.
(7) Les masses pulmonaires peuvent être parenchymateuses, pleurales ou des voies aériennes. Les lésions kystiques à contenu liquidien évoquent les kystes bronchogéniques, les abcès ou les kystes hydatiques. Les tumeurs des voies aériennes s’expriment le plus souvent par des symptômes respiratoires liés à une obstruction ou des hémoptysies pour les tumeurs malignes, représentées principalement par les tumeurs carcinoïdes et mucoépidermoïdes. Parmi les lésions bénignes, il faut citer les hémangiomes, les papillomes et les tumeurs pseudo-inflammatoires ou myofibroblastiques. Celles-ci sont rares mais sont les plus fréquentes des tumeurs bronchiques de l’enfant. Elles se développent dans la lumière bronchique ou à son contact. Enfin, les pleuropneumoblastomes sont des tumeurs malignes à point de départ pleural ou pulmonaire, dont les types II se caractérisent par l’association d’une composante solide et kystique qui devient purement solide dans les types III.
Pour l’ensemble des tumeurs citées, l’imagerie permet d’évoquer un diagnostic, mais seule l’histologie permet le diagnostic de certitude. La prise en charge des patients dépendra du diagnostic évoqué avec concertation entre radiologues, pédiatres et chirurgiens.
Conclusion
Les masses thoraciques regroupent de très nombreuses entités. La possibilité de tumeurs malignes justifie d’avis rapides radiologique et pédiatrique spécialisés. Les signes d’alerte cliniques et la radiographie initiale orientent sur l’imagerie initiale préférentielle avec une place prépondérante du scanner thoracique.
Liens d’intérêts
C. Thumerelle déclare des essais cliniques (en qualité de coinvestigateur, expérimentateur non principal, collaborateur à l’étude) avec AIMMUNE, Alk et Sanofi ; participer à des conférences (invitations en qualité d’intervenant) avec Novartis.
H. Ducou la Pointe déclare ne pas avoir de liens d’intérêts.
S. Lejeune déclare des essais cliniques en qualité de co-investigateur, expérimentateur non principal, collaborateur à l’étude pour AIMMUNE Therapeutic ; avoir participer à des conférences (invitation en qualité d’intervenant) pour Novartis ; bourse de recherche par AstraZeneca.
Cet article fait partie du supplément Pas à Pas 2021 réalisé avec le soutien institutionnel de Procter & Gamble et Sanofi Pasteur.



Références
Ranganath SH, Lee EY, Restrepo R, Eisenberg RL. Mediastinal masses in children. AJR Am J Roentgenol 2012;198:W197-216.
Carter BW, Benveniste MF, Madan R, Godoy MC, de Groot PM, Truong MT, et al. ITMIG Classification of Mediastinal Compartments and Multidisciplinary Approach to Mediastinal Masses. Radiographics 2017;37:413-36.
Brisse H, Neuenschwander S. Les masses thoraciques de l’enfant. XXXIIIes journées d’enseignement post-universitaire; Hôpital Armand Trousseau 2011.