Vous êtes ici
Thématique:
Puberté précoce
![]()
E. Haïne*
Pole de Diabétologie et Endocrinopédiatrie, ESPIC Hôpitaux pédiatriques de Nice CHU-Lenval, 57 Avenue de la Californie, 06200 Nice *Auteur correspondant - Adresse e-mail : haine.e@pediatrie-chulenval-nice.fr (E. Haïne). Cliquez sur l'image pour l'agrandir.| Article validé par : | |
|
SFP (Société Française de Pédiatrie) SFEDP (Société Française d’Endocrinologie et Diabétologie Pédiatrique) |
|
Introduction
La puberté démarre lorsque l’axe hypothalamo-hypophysogonadique est activé. La sécrétion de Gonadotrophin Releasing Hormone (GnRH) se fait alors de manière pulsatile, sous la dépendance des kisspeptines. Le développement pubertaire est décrit par la classification de Tanner.
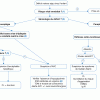
Conduite à tenir devant un démarrage pubertaire précoce
Cette situation concerne 10 fois plus les filles que les garçons.
(1) Chez la fille, le démarrage pubertaire est marqué par l’apparition d’un développement mammaire (S2 selon Tanner). La puberté est définie comme précoce lorsque ce signe apparaît avant l’âge de 8 ans.
(2) Chez le garçon, le démarrage pubertaire est marqué par l'augmentation du volume testiculaire >= 4mL, ou de la longueur > 25 mm (G2 selon Tanner). La puberté est définie comme précoce lorsque ce signe apparaît avant l’âge de 9 ans.
(3) En cas de puberté précoce, la vitesse de croissance s’accélère sous l’effet des stéroïdes sexuels. Elle atteint en moyenne 7 à 8 cm/an pour les filles, 9 à 10 cm/an pour les garçons.
(4) L’âge osseux (défini selon l’atlas de Greulich et Pyle à partir d’une radiographie de main et poignet gauche de face) est alors avancé, de plus de 1 à 2 ans par rapport à l’âge civil. Il peut permettre d’évaluer le pronostic de taille finale, même si sa précision est faible.
(5) L’échographie pelvienne chez la fille recherche des signes d’oestrogénisation des organes génitaux internes (OGI), à savoir : hauteur utérine > 35 mm, présence d’une ligne de vacuité utérine, volumes des ovaires > 2 mL, ovaires multifolliculaires, renflement du corps de l’utérus par rapport au col (rapport corps/col > 1).
(6) Le test au Luteinizing Hormone Releasing Hormone (LHRH) (dosage des gonadotrophines hormone lutéinisante [LH] et hormone folliculo-stimulante [FSH] après injection IV de LHRH) permet de préciser l’origine de la puberté. La réponse typique en période prépubertaire est une réactivité de réponse prédominante en FSH. Lors d’une puberté centrale, la réactivité de réponse prédomine en LH qui s’élève au-delà de 5 mUI/mL ± un ratio LH/FSH > 1. Lors d’une puberté périphérique, la réactivité de réponse en FSH et LH est faible ou nulle.
(7) Chez la fille, le dosage de l’oestradiol n’a aucun intérêt car la sécrétion est pulsatile. Une valeur basse n’exclut pas une sécrétion oestrogénique. Si elle est faite, elle doit être mesurée par Radioimmunoassay (RIA) ou par Liquid Chromatography-Mass Spectrometry (LC-MS/MS) si le système dispose d’une sensibilité suffisante. Un taux d’oestradiol > 20 pg/mL est en faveur d’un démarrage pubertaire.
(8) Chez le garçon, le taux de testostérone sérique s’élève progressivement, parallèlement à l’augmentation de volume des testis. Le début pubertaire doit être suspecté devant un taux de testo stérone > 0,7 nmol/L (après extraction puis dosage LC-MS/ MS ou chromatographie + RIA).
(9) La prémature thélarche typique des petites filles de moins de 2 ans débute le plus souvent en période périnatale, le développement mammaire est isolé (P1) évoluant peu par la suite. En cas de doute, une simple échographie pelvienne retrouvant des OGI prépubères permet de poser le diagnostic de prémature thélarche isolée. L’âge osseux concorde alors à l’âge civil. En dehors de la période périnatale, si un test à la LHRH est réalisé, il montre une réponse avec un pic de FSH supérieur à celui de la LH, ces pubertés peuvent être lentement évolutives et ne pas nécessiter de traitement sous réserve d’une surveillance régulière.
(10) La puberté précoce centrale (PPC) idiopathique représente 92 % des PPC de la fille, mais seulement 50 % des PPC du garçon. Les causes organiques regroupent les tumeurs hypothalamiques (hamartomes, gliomes, astrocytomes, etc.), les malformations cérébrales impliquant l’hypothalamus, les lésions neurologiques postirradiations ou infectieuses, par exemple. Une imagerie par résonance magnétique (IRM) hypothalamohypophysaire doit être réalisée.
(11) Le traitement des PPC est indiqué lorsque la puberté est évolutive (évolutivité clinique, échographique, avance d’âge osseux > 2 ans) et confirmée par le test au LHRH. Un analogue de la GnRH (aGnRH) en injection intramusculaire (IM) toutes les 4 à 12 semaines est habituellement poursuivi jusqu’à un âge normal de démarrage pubertaire.
(12) Une puberté précoce d’origine périphérique, c’est-à-dire de cause ovarienne ou testiculaire, ou secondaire à une tumeur à hormone chorionique gonadotrope (hCG), est suspectée devant une absence de réactivité de sécrétion de LH et de FSH lors du test au LHRH.
(13) L’imagerie abdominopelvienne ou testiculaire oriente le diagnostic.
(14) Chez la fille, le syndrome de McCune-Albright associe entre autres des kystes ovariens sécrétant de l’oestradiol de manière autonome, des taches cutanées café au lait à bords émiettés et des lésions de dysplasie osseuse des os longs.
(15) Les tumeurs ovariennes sécrétantes comprennent les tumeurs des cellules de la granulosa, les tumeurs des cellules de Leydig-Sertoli et les tumeurs du stroma. Elles peuvent être à l’origine d’une puberté précoce périphérique ou d’une pseudopuberté précoce avec virilisation par sécrétion d’androgènes.
(16) Les tumeurs testiculaires sont dominées par celles à cellules de Leydig et par celles à composante germinale.
(17) La testotoxicose est secondaire à une mutation constitutive activatrice du récepteur de la LH.
(18) Dans le cas des tumeurs à hCG (ligne médiane, hépatiques), l’hCG se fixe au récepteur à la LH et induit des pubertés précoces périphériques uniquement chez les garçons avec une augmentation bilatérale du volume testiculaire.
(19) Face à une pilosité pubienne ou axillaire et de l’acné, il peut s’agir d’une simple prémature adrénarche, variante de la normale, mais l’enjeu est d’éliminer une pseudo-puberté précoce.
(20) Les productions anormales d’androgènes se présentent par des signes cliniques d’hyperandrogénie sans développement des seins ni du volume testiculaire mais associent une accélération de la vitesse de croissance et une avance d’âge osseux. Les signes cliniques d’hyperandrogénie comprennent une apparition de pilosité pelvienne et/ou axillaire, de l’acné, une transpiration malodorante, ainsi que chez le garçon l’augmentation de taille de la verge (> 5 cm) et des modifications du scrotum, et chez la fille une hypertrophie clitoridienne.
(21) Le dosage des androgènes de base (testostérone, 17 OH progestérone, sulfate de déhydroépiandrostérone [SDHA] et Δ4Androstènedione [Δ4A]) le matin à 8 heures, ou après stimulation par injection d’Adreno-Cortico-Trophic Hormone (ACTH) lors du test au Synacthène®, permet de confirmer l’hyperandrogénie.
(22) Les taux d’androgènes sont élevés en cas d’hypersécrétion gonadique ou surrénalienne tumorale ou par bloc enzymatique (forme non classique d’hyperplasie congénitale des surrénales). Une exploration complémentaire par scanner ou IRM abdominal (et échographie testiculaire chez le garçon) cherchera un corticosurrénalome, une tumeur gonadique. Le diagnostic de bloc enzymatique sera confirmé par des analyses génétiques.
(23) En cas de prémature adrénarche, il n’y a pas d’accélération marquée de la vitesse de croissance, pas d’augmentation de taille de la verge ni du clitoris, pas d’avance d’âge osseux majeur. Parmi les androgènes, seul le sulfate de DHA (SDHA) peut être légèrement élevé.
Conclusion
La puberté précoce est définie par l’apparition de seins chez la fille avant 8 ans, l’augmentation du volume testiculaire avant 9 ans chez le garçon. Elle peut être centrale ou périphérique. La puberté précoce centrale est idiopathique dans la majorité des cas chez les filles, et organique dans la moitié des cas chez les garçons. Si elle est évolutive, elle sera traitée par agonistes du GnRH. La puberté précoce périphérique est toujours pathologique.
Liens d’intérêts
L’auteur déclare ne pas avoir de liens d’intérêts pour cet article.


Références
Carel JC, Eugster EA, Rogol A, Ghizzoni L, Palmert MR; Conference Group and on behalf of the members of the ESPE-LWPES GnRH Analogs Consensus. Consensus Statement on the Use of Gonadotropin-Releasing Hormone Analogs in Children. Pediatrics 2009;123(4):e752-62. Epub 2009 Mar 30.
Cartault A, Caula-Legriel S, Baunin C, Le Mandat A, Lemasson F, Galinier P, et al. Ovarian masses in adolescent girls. Endocr Dev 2012;22:194-207. Epub 2012 Jul 25.
Carel JC, Léger J. Clinical practice. Precocious puberty. N Engl J Med 2008;358(22):2366-77.
Sultan C, Gaspari L, Maimoun L, Kalfa N, Paris F. Disorders of puberty. Best Pract Res Clin Obstet Gynaecol 2018;48:62-89.