Vous êtes ici
Thématique:
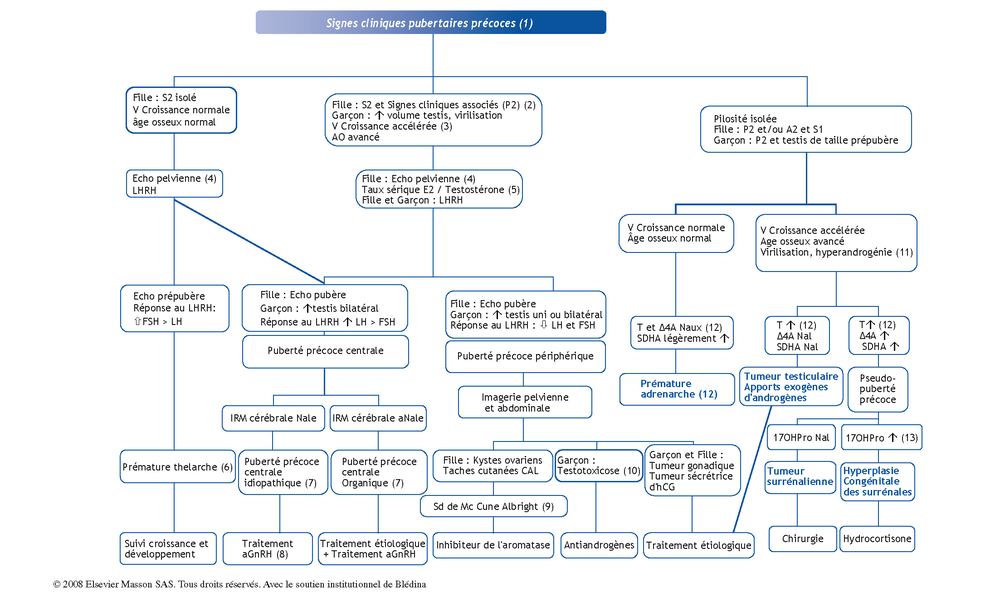
Conduite à tenir devant un développement pubertaire précoce
S. Baron1, F. Despert2
1Clinique Médicale Pédiatrique, Hôpital Mère et Enfant, 44093 Nantes ;2Pédiatrie, Hôpital de Clocheville, 37000 ToursAuteur correspondant - Adresse e-mail : sabine.baron@chu-nantes.fr (S. Baron)Cliquez sur l'image pour l'agrandir.
Arbre décisionnel - Commentaires
(1) Le premier signe de développement pubertaire est l’augmentation de volume des gonades (chez le garçon volume des testis > 4 ml, longueur > 25 mm (G2 selon Tanner), contemporain d’un développement mammaire (S2 selon le stade de Tanner) chez la fille. La puberté est définie comme précoce lorsque ces signes apparaissent avant 8 ans chez la fille et 9 ans chez le garçon. Cette situation est beaucoup plus fréquente chez la fille.
(2) Les signes cliniques pubertaires associés chez la fille peuvent être : une pilosité pubienne (P2) et/ou axillaire (A2), des leucorrhées, des métrorragies (accompagnant les premiers signes pubertaires dans moins de 10% des cas, penser également en cas de métrorragies isolées aux corps étrangers ou tumeurs vaginales, vaginoscopie au moindre doute). Chez le garçon, les testis étant stimulés, augmentent de volume (G2), puis la taille du pénis augmente (> 50 mm), le scrotum se modifie (taille, texture, pigmentation), et la pilosité apparaît (P2 et /ou A2).
(3) La vitesse de croissance s’accélère sous l’effet des stéroïdes sexuels, plus précocement chez la fille. Elle atteint alors 7 à 8 cm/an (> +2DS pour l’âge de 5 à 9 ans). L’âge osseux (défini selon l’atlas de Greulich et Pyle à partir d’une radiographie de main et poignet gauche) s’avance, à > + 2DS pour l’âge, habituellement de plus de 1 à 2 ans par rapport à l’âge civil. Il permet de calculer le pronostic de taille final, qui risque d’être réduit par le développement pubertaire précoce.
(4) L’échographie pelvienne permet, de façon non invasive, d’évaluer le degré d’œstrogénisation des organes génitaux internes (OGI). Le démarrage pubertaire est caractérisé par une augmentation de taille des ovaires (diamètre > 20 mm) mutifolliculaires, et un renflement du corps de l’utérus par rapport au col (rapport corps/col > 1). La hauteur utérine augmente à plus de 30-35 mm, et la ligne de vacuité utérine apparaît.
(5) Le dosage d’œstradiol (E2) sérique n’a pas une sensibilité suffisante pour établir le diagnostic de puberté chez la fille, contrairement au garçon chez qui le taux de testostérone (T) sérique s’élève progressivement, parallèlement à l’augmen-tation de volume des testis. Le début pubertaire correspond habituellement à un taux de testostérone > 0,5-1 ng/ml. Le dosage des gonadotrophines LH et FSH après injection IV de LHRH permet de préciser l’origine de la puberté. La réponse ty-pique en période prépubertaire est prédominante en FSH. Lors d’une puberté centrale la réponse est prédominante en LH (LH > 6 mUI/ml). Lors d’une puberté périphérique la réponse en FSH et LH est faible ou nulle.
(6) La prémature thelarche typique des petites filles de < 2 ans débute le plus souvent en période périnatale, le développement mammaire évoluant peu par la suite. En cas de doute une simple échographie pelvienne retrouvant des OGI prépubères permet de poser le diagnostic de prémature thelarche isolée. Cette situation, pour des filles habituellement plus âgées, peut être la première manifestation d’une puberté précoce centrale et nécessite une surveillance clinique des signes pubertaires et de la croissance.
(7) La puberté précoce centrale (PPC) idiopathique représente 80 % des PPC de la fille, mais seulement 40 % chez le garçon. Les causes organiques sont neurologiques (encéphalopathie, TC,…) ou tumorales (hamartome, astrocytome, gliome,…).
(8) Le traitement des PPC est indiqué lorsque la puberté est évolutive (signes cliniques, échographiques, AO > 2 ans) confirmée par le test au LHRH. Un agonistes du GnRH en injection IM toutes les 4 à 12 semaines est habituellement poursuivi 2 ans ou plus, en fonction de l’âge, de l’AO et du pronostic de taille.
(9) Le syndrome de Mc Cune Albright est dû à une mutation somatique activatrice de la protéine Gsaconstitutives de certains récepteurs hormonaux, en particulier LH. Il associe des taches cutanées café au lait et des lésions de dysplasie osseuse des os longs.
(10) La testotoxicose est due à une mutation constitutive activatrice du récepteur de la LH.
(11) Chez le garçon les signes de virilisation comprennent l’augmentation de taille de la verge (> 5 cm) et des modifications du scrotum, chez la fille une hypertrophie clitoridienne, et une acné.
(12) Les taux sériques d’androgènes permettent le diagnostic étiologique. Seul le Sulfate de DHA (SDHA) est légèrement élevé en cas de prémature adrenarche : cette situation isolée, sans signe de virilisation nécessite une simple surveillance. Les taux de Testostérone (T), SDHA et Δ4Androstènedione (Δ4A) sont élevés en cas d’hypersécrétion surrénalienne tumorale ou par bloc enzymatique, une exploration complémentaire par scanner abdominal et test au Synacthène® est alors indiquée.
(13) Le diagnostic de la forme non classique de l’hyperplasie congénitale des surrénales (le plus fréquent par déficit en 21Hydroxylase) est fait sur le dosage de base ou après Synacthène® de 17OHProgestérone (17OHPro) > 15 ng/ml. La forme plus rare de bloc en 11Hydroxylase est suspectée sur des taux prédominant de Δ4A avec un rapport Δ4A/17OHPro > 1.


Références
Bourguignon JP, Rosenfeld RL. Precocious breast development in a girl, in a boy, and precocious pubarche. In Hochberg Z, editor. Practicals algorithms in pediatric endocrinology. Karger Editor Basel ; 2007.
Brauner R. Puberté pathologique. EMC Pédiatrie. Elsevier Paris ; 2006,4-107-B15.
Léger J. Anomalies de la puberté, Endocrinologie et diabète de l’enfant. In Bourillon A. Pédiatrie pour le praticien. Masson Editor Paris ; 2008, p.271-273.
Limal JM, Coutant R. Avances pubertaires. In Bougnères P, editor. Puberté et croissance. Doin Editeurs Paris ; 1999, p.9-31.