Vous êtes ici
Thématique:
Gros reins hyperéchogènes en anténatal
![]()
C. Rousset-Rouvière
Service de pédiatrie multidisciplinaire, AP-HM, Marseille, France*Auteur correspondant - Adresse e-mail : caroline.rousset-rouviere@ap-hm.fr (C. Rousset-Rouvière). Cliquez sur l'image pour l'agrandir.
| Article validé par : | |
|
SFIPP (Société Francophone d’Imagerie Pédiatrique et Prénatale) |
|
|
SFN (Société Française de Néonatalogie) |
|
|
SNP (Société de Néphrologie Pédiatrique) |
|
| Remerciements aux relecteurs : | |
|
M. Alison (SFIPP) E. Kermorvant (SFN), J. Bacchetta O. Gillion-Boyer L. Heidet M. Tsimaratos (SNP) |
|
Introduction
Le diagnostic prénatal (DPN) de gros reins hyperéchogènes est une situation difficile avec un enjeu double : étiologique et pronostique. La découverte est habituellement tardive au cours du 2e ou 3e trimestre de grossesse.
Les reins sont dits « hyperéchogènes » lorsque leur échogénicité est supérieure à celle du foie ou de la rate. L’hyperéchogénicité, non spécifique d’une pathologie rénale, résulte souvent de la présence de microkystes indétectables en échographie, de dysplasie ou de dilatation tubulaire.
La néphromégalie est définie par une taille de reins supérieure à +2DS.
L’échographie foetale ne permet pas de préciser l’étiologie dans de nombreux cas mais reste l’examen clé pour évaluer le pronostic rénal. Il faudra exclure en premier lieu une uropathie obstructive. Le diagnostic est ensuite orienté en fonction des antécédents familiaux de pathologies rénales ainsi que de l’existence de malformations extrarénales associées.
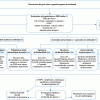
Conduite à tenir devant des gros reins hyperéchogènes en anténatal
Démarche diagnostique générale
(1) Il faudra en premier lieu exclure une uropathie obstructive (dilatation des cavités pyélocalicielles, des uretères, étude de la vessie, etc.).
(2) L’échographie anténatale doit préciser l’aspect des reins avec une sonde de haute fréquence (si les conditions techniques le permettent) : taille des reins, échogénicité du parenchyme, différenciation cortico-médullaire (DCM), kystes (nombre, taille, localisation), quantité de liquide amniotique (LA), et rechercher des malformations extrarénales.
L’échographie peut être complétée par une IRM foetale permettant de préciser la localisation des kystes (meilleure résolution en contraste mais moins bonne résolution spatiale que l’échographie), les atteintes extrarénales et éliminer les anomalies du tractus urinaire.
(3) La recherche d’antécédents familiaux de maladie rénale et la réalisation d’un arbre généalogique sont primordiales. Une échographie rénale sera demandée aux deux parents, voire aux grands-parents lorsque les parents sont jeunes, car les kystes peuvent apparaître tardivement. L’existence de maladie kystique rénale de transmission verticale doit orienter en premier lieu vers une polykystose rénale autosomique dominante (PKRAD) : voir 5a. Une anomalie du gène HNF1β doit être évoquée en cas de diabète MODY ou hyperuricémie dans la famille : voir 5b. Une consanguinité doit être recherchée.
(4) La réalisation d’un caryotype est systématique s’il existe des atteintes extrarénales. Elle se discute dans les autres cas, en fonction des éléments d’orientation étiologique.
(5) Causes à évoquer devant des gros reins hyperéchogènes isolés en anténatal
(5a) La PKRAD est la maladie rénale héréditaire la plus fréquente et touche environ 1 nouveau-né sur 1 000. Elle est due à des variations pathogènes de PKD1 dans 85 % des cas et de PKD2 dans 15 % des cas. Plus récemment, des variations de GANAB et DNAJB11 ont été décrites dans des formes atypiques de PKRAD. Elle se révèle le plus souvent à l’âge adulte, mais les formes anténatales sont possibles. L’aspect typique anténatal est celui de reins modérément augmentés de taille, avec une hyperéchogénicité corticale et une quantité de LA souvent normale. La DCM apparaît accentuée. Parfois, des kystes sont visibles. Ils sont le plus souvent corticaux mais peuvent être corticomédullaires. En dehors de rares formes sévères avec énormes reins hyperéchogènes et oligo-anamnios pouvant conduire à une demande d’interruption de grossesse, les enfants présentent peu de complications de la maladie dans la petite enfance. L’évolution se fera progressivement vers l’insuffisance rénale terminale à un âge variable. Les manifestations extrarénales, qui incluent des anévrismes intracérébraux, des valvulopathies et des kystes dans d’autres organes comme le foie, ne se détectent pas en anténatal. Les formes de découverte anténatale concernent presque exclusivement le gène PKD1 ou le syndrome des gènes contigus TSC2-PKD1 (délétion simultanée des gènes PKD1 et TSC2 impliqué dans la sclérose tubéreuse de Bourneville).
(5b) Le gène HNF1β (TCF2) code pour le facteur de transcription HNF1β qui joue un rôle dans le développement embryonnaire de divers organes incluant le rein, le foie, le pancréas et les organes génitaux. Les variations pathogènes du gène HNF1β, transmises sur un mode autosomique dominant, sont responsables d’un phénotype rénal variable (hypo- ou dysplasie, agénésie, kystes, etc.) pouvant être associé à des atteintes extrarénales comme une hypoplasie du pancréas, un diabète MODY, des malformations génitales, une hyperuricémie, des anomalies du bilan hépatique ou une hypomagnésémie. Des anomalies neurocognitives variables sont décrites. Dans certaines séries, la néphropathie liée au gène HNF1β est la première cause de reins hyperéchogènes en anténatal. Le plus souvent les reins sont de taille normale avec ou sans microkystes corticaux et la quantité de LA est normale. Mais parfois le tableau peut mimer celui d’une polykystose rénale autosomique récessive avec de gros reins hyperéchogènes dédifférenciés et un oligoamnios. Les anomalies extrarénales sont exceptionnellement détectées en anténatal. Les antécédents familiaux peuvent orienter le diagnostic lorsqu’il ne s’agit pas d’une mutation de novo. Il existe une grande variabilité interfamiliale mais aussi intrafamiliale rendant le DPN encore plus difficile. Le pronostic rénal à long terme est variable, mais une insuffisance rénale terminale dès l’enfance est possible.
(5c) La polykystose rénale autosomique récessive (PKRAR) touche environ 1 nouveau-né sur 20 000 et est le plus souvent détectée en anténatal. Elle est due à des variants bi-alléliques dans le gène PKHD1 (polycystic kidney and hepatic disease 1) et est transmise selon un mode autosomique récessif. Elle associe une maladie kystique rénale par atteinte des tubes collecteurs et une atteinte hépatique de type fibrose hépatique congénitale. Les formes sévères se présentent avec de très gros reins (souvent de taille supérieure à +4DS) hyperéchogènes avec perte de la DCM et oligo-anamnios, au 2e trimestre de grossesse. La présentation est cependant variable avec parfois des reins modérément augmentés de taille et un LA faiblement diminué. L’hyperéchogénicité, classiquement médullaire, peut être aussi globale. La visualisation de macrokystes rénaux est rare et l’atteinte hépatique n’est pas visible en anténatal. Le phénotype est variable mais un décès en période périnatale ou durant la première année de vie concerne jusqu’à 30 % des cas. Passé cette période, environ la moitié des enfants développe une insuffisance rénale chronique terminale au cours de la première décennie. Les manifestation hépatiques sont de gravité variable et peuvent évoluer vers une hypertension portale. Le génotypage prénatal est possible quand la mutation a été préalablement identifiée chez un cas index.
(6) Causes à évoquer devant des gros reins hyperéchogènes pouvant être associés à des atteintes extrarénales en anténatal
(6a) Le syndrome de Bardet-Biedl est une maladie autosomique récessive rare dont la prévalence est comprise entre 1/120 000 et 1/170 000. Une vingtaine de gènes sont impliqués dans cette maladie. Elle est caractérisée par une obésité, une rétinite pigmentaire, une polydactylie post-axiale, un hypogonadisme, une atteinte rénale et un retard mental variable. D’autres malformations (cardiaques, génitales, etc.) peuvent être associées. L’atteinte rénale est très hétérogène : kystes, ectopie, rein en fer à cheval, aplasie, reflux vésico-urétéral, etc. En anténatal, elle peut se manifester par de gros reins hyperéchogènes avec perte de la DCM avec ou sans macrokystes pouvant mimer une PKRAR ou une PKRAD. La quantité de LA est variable selon la gravité de l’atteinte rénale. L’existence d’atteintes extrarénales comme une polydactylie post-axiale peut orienter le diagnostic, mais elle manque dans environ 30 % des cas.
(6b) Le syndrome de Meckel-Gruber, de transmission autosomique récessive, a une prévalence estimée entre 1 et 10 cas pour 150 000 naissances. Il est caractérisé par une dysplasie kystique rénale associée à une atteinte du système nerveux central (encéphalocèle occipitale le plus souvent), une pathologie de la plaque ductale et une polydactylie. D’autres atteintes comme un raccourcissement des os longs, des malformations cardiaques et des organes génitaux, une microphtalmie et une fente labio-palatine peuvent être présentes. En anténatal, devant de gros reins hyperéchogènes avec ou sans kystes médullaires, un oligoamnios, des anomalies du système nerveux central et des anomalies des extrémités, il faudra l’évoquer en premier lieu. Dans la plupart des cas, l’évolution se fera vers une mort foetale in utero.
(6c) D’autres atteintes syndromiques peuvent être plus rarement diagnostiquées devant de gros reins hyperéchogènes anténatals. On peut citer : le syndrome de Beckwith-Wiedemann (macrosomie, macroglossie, omphalocèle, hémi-hypertrophie corporelle, dysplasie kystique médullaire rénale), le syndrome d’Ivemark type II (dysplasie rénale, fibrose pancréatique et dysgénésie hépatique associées à des anomalies squelettiques et une anencéphalie), le syndrome de Jarcho-Levin (anomalies squelettiques associées à des atteintes rénales, génitales, cardiaques et du système nerveux central), le syndrome de Beemer (côtes courtes, micromélie, polydactylie, malformation rénale, etc.) ou la sclérose tubéreuse de Bourneville (tumeurs bénignes multisystémiques touchant notamment la peau, le cerveau, le rein, le poumon et le coeur).
(6d) Des anomalies chromosomiques telles que la trisomie 13, 18 ou 21 peuvent donner des reins hyperéchogènes de taille normale ou augmentée, associés à des atteintes extrarénales comme des malformations cérébrales (holoprosencéphalie), cardiaques ou génitales, une omphalocèle ou une polydactylie.
(7) Enfin, d’autres étiologies s’exprimant plus rarement en anténatal peuvent être évoquées devant des reins hyperéchogènes de taille normale ou augmentée. C’est le cas de certaines maladies métaboliques comme l’acidurie glutarique de type II (déficit multiple en acyl-CoA déshydrogénase) responsable de coma acidosique, hyperammoniémie, hypotonie et ataxie, myocardiopathie, épilepsie, reins polykystiques et dysmorphie faciale ; ou le CDG-syndrome (déficit enzymatique touchant la synthèse des glycoprotéines) responsable d’atteintes multiviscérales. Certains syndromes néphrotiques congénitaux peuvent donner de gros reins hyperéchogènes en anténatal, notamment lorsque les gènes WT1, CRB2 ou NPHS1 sont impliqués. De rares cas de thrombose des veines rénales peuvent s’exprimer en anténatal et donner un tableau de reins hyperéchogènes plus ou moins augmentés de taille mais le plus souvent l’anomalie est unilatérale et s’associe à un hématome de la surrénale. Les dysgénésies tubulaires congénitales ou acquises (secondaire à la prise maternelle d’inhibiteurs de l’enzyme de conversion) sont caractérisées en anténatal par des reins hyperéchogènes (ou d’échogénicité subnormale) mais le plus souvent de taille normale ou peu augmentée ; il s’y associe un RCIU, un oligoamnios et une hypocalvaria (hypoplasie des os du crâne). Les variants du gène SLC34A1 (codant pour le transporteur Npt2a) responsables d’une hypercalcémie infantile et néphrocalcinose peuvent donner en anténatal des reins hyperéchogènes de taille normale ou peu augmentée. Des cas d’hyperéchogénicité transitoire avec ou sans néphromégalie sont décrits ; il faudra observer une normalisation des échographies foetales au cours du suivi ou après la naissance pour confirmer ce diagnostic.
(8) Évaluation multidisciplinaire
Dans tous les cas, une discussion en centre pluridisciplinaire de diagnostic prénatal (CPDPN) doit être faite en la présence d’obstétriciens, de radiologues, de généticiens, de néonatologues et de néphropédiatres afin de donner un conseil prénatal éclairé aux parents et les accompagner dans leur décision. Un diagnostic moléculaire prénatal en cas de variant identifié dans la famille peut se discuter pour certaines pathologies. On proposera une planification de la naissance en maternité de type III ou un accès facile à une équipe de néphropédiatres en fonction de la gravité du tableau.
L’évaluation pronostique de la fonction rénale postnatale est primordiale. Même pour une maladie connue, elle reste complexe en raison de la grande variabilité phénotypique. Peu de marqueurs foetaux prédictifs sont disponibles ; cette évaluation repose avant tout sur des critères échographiques et la surveillance de l’évolutivité des anomalies au cours de la grossesse. Un taux anormal de bêta-2 microglobuline (dans les urines ou le sang foetal) est associé à un pronostic sombre, mais des valeurs normales ne permettent pas d’exclure une insuffisance rénale postnatale. Les formes les plus graves, à haut potentiel létal in utero ou à la naissance, s’accompagnent d’un anamnios précoce responsable d’hypoplasie pulmonaire et d’arthrogrypose (séquence de Potter). Dans les formes sévères (oligoamnios modéré à sévère, très gros reins dédifférenciés) ou en présence de malformations extrarénales graves, une demande parentale d’interruption de grossesse est le plus souvent acceptée. L’examen foetopathologique pourra orienter le diagnostic étiologique et aider l’interprétation des études moléculaires. Dans les formes de gravité intermédiaire et en l’absence d’éléments susceptibles d’orienter vers un diagnostic étiologique de certitude, le conseil est souvent complexe.
Conclusion
La découverte de gros reins hyperéchogènes en anténatal est une situation complexe. En l’absence d’antécédents familiaux précis, le diagnostic étiologique n’est pas toujours aisé. En dehors des formes les plus sévères (gros reins dédifférenciés avec oligoanamnios précoce et/ou atteintes extrarénales sévères) dans lesquelles une demande d’interruption de grossesse est le plus souvent acceptée, on ne dispose pas de marqueurs fiables en routine permettant de prédire précisément le devenir rénal à long terme. S’ajoute à cela une grande variabilité phénotypique interet intrafamiliale compliquant le conseil génétique. Une discussion au cas par cas en CPDPN est indispensable.
Liens d’intérêts
L’auteur déclare ne pas avoir de liens d’intérêts.
Cet article fait partie du supplément Pas à Pas 2021 réalisé avec le soutien institutionnel de Procter & Gamble et Sanofi Pasteur.


Références
Le Guern H, Collet M, Jehannin B, Boog G. Le rein foetal, pathologie, sémiologie échographique et corrélations pré- et postnatales. JEMU 1983.
Emmanuelli V, Lahoche-Manucci A, Holder-Espinasse M, Devisme L, Vaast P, Dieux-Coeslier A, et al. Diagnostic anténatal des reins hyperéchogènes : à propos de 17 cas. J Gynecol Obstet Biol Reprod 2012.
Chaumoitre K, Brun M, Cassart M, Maugey-Laulom B, Eurin D, Didier F, et al. Differential diagnosis of fetal hyperechogenic cystic kidneys unrelated to renal tract anomalies: a multicenter study. Ultrasound Obstet Gynecol 2006.
Decramer S, Parant O, Beaufils S, Clauin S, Guillou C, Kessler S, et al. Anomalies of the TCF2 gene are the main cause of fetal bilateral hyperechogenic kidneys.J Am Soc Nephrol 2007.
Tsatsaris V, Gagnadoux MF, Aubry MC, Gubler MC, Dumez Y, Dommergues M. Prenatal diagnosis of bilateral isolated fetal hyperechogenic kidneys. Is it possible to predict long term outcome?. BJOG 2002.
Gimpel C, Avni FE, Bergmann C, Cetiner M, Habbig S, Haffner D, et al. Perinatal diagnosis, management, and follow-up of cystic renal diseases: a clinical practice recommendation with systematic literature reviews. JAMA Pediatr 2018.