Vous êtes ici
Thématique:
Gynécomastie chez l’enfant et l’adolescent
![]()
A. Lusteau1, C. Villanueva1, CL. Gay1, K. Perge1,2
1Service de diabétologie et d’endocrinologie pédiatrique, Hospices civils de Lyon, Hôpital Femme Mère Enfant, Bron, France 2Université Claude-Bernard, Lyon 1, Lyon, France Auteur correspondant - Adresse e-mail : kevin.perge@chu-lyon.fr (K. Perge). Cliquez sur l'image pour l'agrandir.| Article validé par : | |
|
Société Française d’Endocrinologie et Diabétologie Pédiatrique (SFEDP) |
|
Introduction
(1) La gynécomastie est une prolifération bénigne de la glande mammaire chez l’homme. Elle résulte d’un déséquilibre entre l’action des oestrogènes et des androgènes. À l’examen clinique (patient allongé sur le dos, les mains derrière la nuque, palpation au moyen du pouce et de l’index), la gynécomastie apparaît comme une masse tissulaire, élastique, molle ou ferme, non indurée, centrée sur le mamelon et l’aréole, sans atteinte de la peau en regard ni rétraction du mamelon ni atteinte ganglionnaire. La douleur spontanée ou provoquée à la palpation est souvent fréquente au cours des six premiers mois après son apparition et ne constitue pas un signe de gravité. La gynécomastie est une situation fréquente du petit enfant et de l’adolescent pubère. L’objectif de l’interrogatoire et de l’examen clinique est d’éliminer les causes de gynécomasties non physiologiques.
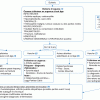
Orientation diagnostique devant une gynécomastie chez l’enfant ou l’adolescent
(2) Les deux diagnostics différentiels de la gynécomastie sont :
• l’adipomastie : dépôt de graisse sous-aréolaire, fréquemment retrouvée en situation de surpoids ou d’obésité, ne se manifestant pas comme une masse tissulaire (absence de prolifération glandulaire).
• le carcinome mammaire : diagnostic très rare chez l’enfant, se présentant comme une masse généralement unilatérale, ferme voire indurée, indolore, souvent excentrée par rapport au mamelon, pouvant être associée à un des quatre signes suivants : dépression de la peau, rétraction du mamelon, écoulement et adénopathies axillaires.
La distinction entre gynécomastie, adipomastie et carcinome mammaire est essentiellement clinique. En cas de difficulté, une échographie mammaire peut être indiquée.
(3) La première étape de l’enquête étiologique est l’interrogatoire.
• Il faut rechercher la prise de médicaments toxiques ou topiques locaux qui par leur action soit oestrogénique soit antiandrogénique, soit de mécanisme encore inconnu, est une cause fréquente de gynécomastie (liste non exhaustive dans le tableau 1). Une attention particulière sur la consommation de produits dit « naturels » en vente libre (huile pour la peau, produits à base de plantes) est essentielle chez l’enfant. Une vigilance sur la prise de toxiques (cannabis) ou de produits dopants (stéroïdes anabolisants) est indispensable chez l’adolescent.
• Les antécédents du patient renseignent sur une pathologie connue : insuffisance rénale chronique (mécanisme multifactoriel dont un hypogonadisme par dysfonction des cellules de Leydig et une hyperprolactinémie), hépatopathie (augmentation de la SHBG [Sex Hormone Binding Protein] et diminution du catabolisme des androgènes), hyperthyroïdie (augmentation de la SHBG et augmentation de l’activité de l’aromatase).
| Par augmentation de la production d’oestrogènes | Par diminution de la synthèse/action de la testostérone |
| • OEstrogènes • Gonadotrophines • Phénytoïne • Estramustine |
• Acétate de cyprotérone • Kétoconazole • Metronidazole • Spironolactone, éplérénone • Anti-ulcéreux : cimétidine, ranitidine, oméprazole • Inhibiteurs de la 5-alpha-réductase :dutastéride, finastéride • Anti-tumoraux : busulfan, sorafénib, imatinib, mitotane • Anti-androgènes non stéroïdiens utilisés dans le cancer de la prostate :bicalutamide, enzalutamide, flutamide • Traitement anti-VIH : éfavirenz, antiprotéases • Médicaments provoquant une hyperprolactinémie :antipsychotiques, antiémétiques (alizapride, dompéridone) |
| Mécanisme non connu | |
| • Toxiques et stupéfiants : alcool, cannabis, amphétamines, héroïne, méthadone, marijuana • Cétirizine • Antidépresseurs : antidépresseurs tricycliques, miansérine • Antiépileptiques : carbamazépine, acide valproïque • Antagonistes du calcium : vérapamil, nifédipine • Clonidine • Diazépam • Digoxine • Inhibiteurs de la phosphodiestérase de type 5 : sildénafil • Inhibiteurs de la xanthine oxydase : allopurinol, fébuxostat |
|
(4) La deuxième étape de l’enquête étiologique est clinique.
L’examen clé est l’examen pubertaire (classification selon le stade de Tanner), en particulier l’examen du volume testiculaire, pour répondre aux questions suivantes :
• la puberté est-elle débutée (définie par un volume testiculaire ≥ 4 ml mesuré avec l’aide d’un orchidomètre ou une longueur testiculaire ≥ 25 mm) ?
• la puberté est-elle d’évolution normale ?
• existe-t-il une masse ou asymétrie testiculaire devant faire réaliser une échographie testiculaire en urgence ?
(4A) Puberté non débutée (volume testiculaire < 4 ml ou longueur testiculaire < 25 mm).
En l’absence de début pubertaire et en dehors des 6 premiers mois de vie, période de la mini-puberté durant laquelle une gynéco mastie isolée est souvent rencontrée (gynécomastie physio logique), la gynécomastie doit faire rechercher une étiologie (gynécomastie pathologique). En cas d’association à une virilisation et/ou une accélération staturale, une puberté précoce périphérique (« pseudo-puberté précoce ») doit être évoquée. Voir aussi le pas à pas « Puberté précoce ».
(4B) Puberté débutée (volume testiculaire ≥ 4 ml ou longueur testiculaire ≥ 25 mm).
Pendant la puberté normale du garçon, la gynécomastie est fréquente, uni- ou bilatérale, s’installant dans la première année de la puberté ; elle concerne près de 50 % des garçons. Il s’agit d’une gynécomastie physiologique, régressant de manière spontanée entre 6 et 24 mois. Dans sa forme typique, cette gynécomastie péripubertaire ne nécessite pas d’examen complémentaire.
Il faut connaître les signes d’alerte conduisant à suspecter une gynécomastie pathologique :
• signes associés : asymétrie testiculaire, anomalie des organes génitaux externes (OGE : micropénis actuel ou traité, hypospade actuel ou opéré, cryptorchidie actuelle ou opérée), écoulement mammaire ;
• signes de puberté atypique : âge < 9 ans au diagnostic (puberté précoce), absence de progression de la puberté = puberté non évolutive : volume testiculaire restant inférieur à 6 ml à 12 mois de suivi (on parle d’atrophie testiculaire, le passage d’un stade de Tanner à un autre prenant en moyenne 6 à 12 mois), absence de pilosité à 12 mois de suivi ou décalage entre la pilosité et le volume testiculaire, absence de poussée staturale (pic pubertaire) à 24 mois de suivi ;
• persistance de la gynécomastie au-delà de 24 mois.
(5) L’enquête paraclinique minimale à réaliser devant une gynécomastie d’allure pathologique :
• bilan général sont : à la recherche d’une insuffisance rénale chronique, d’une hépatopathie ou d’une hyperthyroïdie : créatininémie, bilan hépatique, TSH ;
• bilan hormonal : LH, FSH, oestradiol, testostérones totale et libre à 8 heures, SHBG, β-hCG.
Ce bilan peut être différé en cas de gynécomastie dans un contexte de pathologie prédisposante ou de prise médicamenteuse, le temps d’apprécier son évolution après le traitement étiologique ou l’arrêt du médicament (régression dans un délai variable, en 24 mois maximum).
(6-7) Les différentes causes de gynécomastie pathologique peuvent être classées selon leur mécanisme physiopathologique.
(6) Diminution de l’ambiance androgénique
- (6A) LH et FSH plasmatiques élevées : hypogonadisme hypergonadotrope = hypogonadisme primaire ou périphérique. Un premier diagnostic à éliminer est le syndrome de Klinefelter par la réalisation d’un caryotype. D’autres causes devront être évoquées par la suite (séquellaire ou dysgénésie gonadique) ;
- (6B) LH et FSH plasmatiques basses : hypogonadisme hypogonadotrope = hypogonadisme central. L’origine peut être congénitale, acquise ou fonctionnelle. Le complément de bilan comprend un dosage de la prolactine (recherche d’une hyperprolactinémie responsable d’une inhibition des gonadotrophines) et une IRM hypothalamo-hypophysaire et des bulbes olfactifs (syndrome de Kallmann).
• Par résistance aux androgènes (testostérones totale et libre augmentées, LH et FSH augmentées) : (6C) syndrome d’insensibilité aux androgènes.
(7) Augmentation de l’ambiance oestrogénique
• β-hCG élevés: (7A) tumeurs germinales (testiculaires, cérébrales, médiastinales, hépatiques…). La gynécomastie est due à une activité de l’aromatase tumorale augmentée et à une stimulation directe par hCG de la production d’oestradiol par les cellules de Leydig. Une échographie testiculaire doit être réalisée devant toute masse ou asymétrie testiculaire ou au moindre doute.
• β-hCG non élevés :
- (7B) production tumorale d’oestrogènes : certaines tumeurs testiculaires, les tumeurs des cellules de Leydig et les tumeurs calcifiées à grandes cellules de Sertoli (LCCSCT), peuvent entraîner une gynécomastie par surexpression de l’aromatase p450 (CYP19A1), ce qui augmente la conversion du delta-4-androstènedione (principal androgène surrénalien chez les garçons prépubères) en oestrone. Les taux d’oestrogènes, d’oestrone, et d’oestra diol, peuvent rester en dessous de la limite de détection des tests standards. Cependant, la sensibilité du cartilage de croissance et du tissu mammaire aux oestrogènes peut entraîner une accélération de la croissance, un âge osseux avancé, et une gynécomastie chez les garçons prépubères. Une échographie testiculaire doit être réalisée devant toute masse ou asymétrie testiculaire ou au moindre doute. Un tiers des LCCSCT sont associées aux syndromes de Carney et de Peutz-Jeghers.
Des tumeurs surrénaliennes, souvent malignes (corticosurrénalomes), peuvent être féminisantes par surproduction d’oestro gènes par la tumeur (augmentation de l’aromatase), et par conversion périphérique des androgènes (déhydroépiandro stérone – DHEA, androstènedione) en oestrogènes dans le tissu adipeux ;
- (7C) production non tumorale d’oestrogènes : d’origine génétique (syndrome d’excès d’aromatase : maladie autosomique dominante rare causée par la surexpression de CYP19A1 codant pour l’aromatase ; les garçons présentent une gynécomastie pré- ou péripubertaire, des gonadotrophines basses, et un âge osseux avancé), ou non génétique par hyperactivité de l’aromatase secondaire à une obésité ou une hyperthyroïdie.
(8) En l’absence d’étiologie retrouvée, la gynécomastie est dite idiopathique. Dans ce cadre, en cas de gêne importante, la prise en charge est chirurgicale.
Conclusion
La gynécomastie est fréquente et physiologique chez le nouveau-né avant 6 mois, et chez l’adolescent en période pubertaire. De nombreux médicaments, toxiques ou topiques locaux, sont associés à une gynécomastie et doivent être recherchés avant tout bilan complémentaire. L’objectif de l’interrogatoire et de l’examen clinique est de détecter les signes d’alerte devant faire rechercher une gynécomastie non physiologique. En cas de signes d’alerte ou de persistance (> 6 mois pour le nouveau-né ou > 24 mois pour l’adolescent pubère), un bilan minimal doit être réalisé comprenant l’évaluation des fonctions rénale, hépatique et thyroïdienne associé à un bilan hormonal (LH, FSH, oestradiol, testostérones totale et libre à 8 heures), SHBG, β-hCG). Les principales urgences étiologiques à éliminer sont d’origine tumorale (germinales, testiculaires et surrénaliennes). En l’absence d’étiologie retrouvée, la gynécomastie est dite idiopathique. Dans ce cadre, en cas de gêne importante, la prise en charge est chirurgicale.
Liens d’intérêts
Les auteurs déclarent ne pas avoir de liens d’intérêts.
Cet article fait partie du supplément Pas à Pas 2023 réalisé avec le soutien institutionnel de Procter & Gamble et Sanofi.


Références
Braunstein GD. Clinical practice. Gynecomastia. N Engl J Med 2007;357(12):1229-37. DOI: 10.1056/NEJMcp070677. PMID: 17881754.
Kanakis GA, Nordkap L, Bang AK, Calogero AE, Bártfai G, Corona G, et al. EAA clinical practice guidelines-gynecomastia evaluation and management. Andrology 2019;7(6):778-93.
Ma NS, Geffner ME. Gynecomastia in prepubertal and pubertal men. Curr Opin Pediatr 2008;20(4):465-70. DOI: 10.1097/MOP.0b013e328305e415. PMID: 18622206.
Meyer P. Évaluation et prise en charge d’une gynécomastie [Evaluation and management of gynecomastia]. Rev Med Suisse 2009;5(198):783-7. French. PMID: 19418981.
Swerdloff RS, Jason Ng CM. Gynecomastia: Etiology, Diagnosis, and Treatment. In: Feingold KR, Anawalt B, Boyce A, Chrousos G, de Herder WW, Dhatariya K, et al., editors. Endotext [Internet]. South Dartmouth (MA): MDText.com, Inc.; 2000.