Vous êtes ici
Thématique:
Diagnostic de la maladie coeliaque chez l’enfant
![]()
H. Lengliné1, A. Fabre2,3
1Service de gastroentérologie et nutrition pédiatriques, CHU Robert-Debré, AP-HP, Paris, France2Aix-Marseille Université, INSERM, MMG, Marseille, France
3Service de pédiatrie multidisciplinaire, Hôpital de La Timone Enfants, AP-HM, Marseille, France
*Auteur correspondant - Adresse e-mail : helene.lengline@aphp.fr (H. Lengliné). Cliquez sur l'image pour l'agrandir. Cliquez sur l'image pour l'agrandir.
| Article validé par : | |
|
GFHGNP (Groupe Francophone d’Hépatologie-Gastroentérologie et Nutrition Pédiatriques) |
|
|
Comité de nutrition de la SFP |
|
| Remerciements aux relecteurs : | |
|
C. Jung (GFHGNP) E. Mas (GFHGNP) N. Peretti (GFHGNP et Comité de nutrition) |
|
Introduction
La maladie coeliaque, ou intolérance au gluten, est une entéropathie auto-immune induite par l’ingestion de gluten, survenant chez des individus génétiquement prédisposés. Elle se déclenche après l’exposition au gluten provenant de produits céréaliers contenant du blé, du seigle, ou de l’orge (et, dans certains cas, de l’avoine). Le gluten est un ensemble de protéines (prolamines et gluténines) insolubles dans l’eau, et ayant des propriétés viscoélastiques. C’est son haut contenu en proline qui est responsable de l’immunogénicité importante du gluten. La maladie coeliaque a certaines caractéristiques d’une maladie auto-immune spécifique d’organe, en particulier le terrain génétique prédisposant, la présence d’autoanticorps tissulaires (antitransglutaminase et antiendomysium) et de cellules cibles (les entérocytes), ainsi que l’association à d’autres maladies auto-immunes. La maladie coeliaque a pour conséquence une inflammation du chorion et une atrophie des villosités intestinales, responsable de signes digestifs et d’une malabsorption.
La maladie coeliaque peut être évoquée devant des tableaux cliniques très variables (PAP 1), chez un enfant ayant déjà été exposé au gluten. Cependant, 90 % des sujets atteints de maladie coeliaque ne présentent pas de symptôme, la maladie coeliaque étant dans ce cas dite silencieuse, ou asymptomatique. De nombreux patients asymptomatiques ignorent d’ailleurs pendant de longues années qu’ils sont atteints de la maladie. Les patients chez qui le diagnostic est posé en l’absence de symptôme sont en général dépistés en raison d’un terrain à risque (PAP 2). Ils doivent être pris en charge de la même manière que les patients symptomatiques car les risques de la maladie à moyen et long terme sont les mêmes, et l’évolution d’une forme silencieuse vers une forme symptomatique est possible.
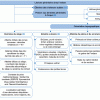
Suspicion de maladie coeliaque chez un enfant symptomatique : démarche diagnostique (PAP 1)
(1) Les signes cliniques de la maladie coeliaque peuvent être très divers. Les signes digestifs typiques sont : une diarrhée chronique, une distension abdominale, des douleurs abdominales, une anorexie, une perte pondérale ou des vomissements.
Il ne faut cependant pas méconnaître le diagnostic de maladie coeliaque devant des symptômes digestifs frustes (constipation) ou devant des signes extradigestifs isolés, surtout chez le grand enfant, une présentation atypique étant possible.
Les signes extradigestifs peuvent être : un retard de croissance, une stagnation, voire une régression des acquisitions psychomotrices, un retard pubertaire ou une aménorrhée, des troubles de l’humeur, une asthénie, une neuropathie périphérique sensitivo-motrice (paresthésies…), une ataxie, des convulsions, des arthralgies, une fragilité osseuse, des anomalies de l’émail dentaire, une dermatite herpétiforme, une carence martiale, ou une élévation des transaminases.
(2) C’est le dosage des IgA antitransglutaminase (anti-TG2) qui est actuellement la sérologie de référence, recommandée en première intention pour le diagnostic de la maladie coeliaque. Ce dosage doit toujours être associé à un dosage des IgA totales pour écarter un déficit en IgA, qui touche environ 5 % des patients coeliaques, mais reste le plus souvent sans expression clinique.
(3) Les IgA antiendomysium (anti-EM) ne doivent être dosées qu’en seconde intention, uniquement selon les indications mentionnées dans l’algorithme diagnostique. Leur résultat est donné en inverse de dilution (par exemple : seuil usuel à 1/40, dilution supérieure suivante 1/80, puis 1/160, etc.). Dans la situation d’un patient symptomatique qui présente un résultat de dosage des anticorps anti-TG2 supérieur à 10 fois la normale (> 10N), il faut compléter le bilan par un dosage des anticorps antiendomysium (anti-EM) sur un deuxième prélèvement.
(4) Si ce dosage est également positif, alors les conditions sont réunies pour affirmer le diagnostic de maladie coeliaque sans nécessité de confirmation histologique, d’après les dernières recommandations de l’ESPGHAN (Société européenne de gastroentérologie pédiatrique) publiées en 2020. Un suivi spécialisé en gastroentérologie pédiatrique doit dans ce cas être mis en place.
(5) Un dosage d’IgA anti-EM peut également être proposé lorsque les IgA anti-TG2 sont négatives (sans déficit en IgA associé) mais qu’il existe une forte suspicion clinique de maladie coeliaque.
(6) Lorsque les conditions clinico-biologiques ne sont pas suffisantes pour affirmer le diagnostic de maladie coeliaque sans biopsie (IgA anti-TG2 positives mais < 10N, ou > 10N avec IgA anti-EM négatives), une endoscopie digestive haute (EDH) doit être réalisée, avec réalisation de biopsies duodénales multiples. Les recommandations actuelles sont de prélever des biopsies multiples, au minimum 4 biopsies duodénales (idéalement 6), dont au moins 1 dans le bulbe, en raison de l’hétérogénéité des lésions.
(7) La maladie coeliaque se caractérise par l’association de 4 types de lésions histologiques, très caractéristiques de cette pathologie lorsqu’ils sont associés :
• Une atrophie villositaire de degré variable : elle peut être partielle, subtotale ou totale (classification de Marsh III A, B ou C).
• Une hyperplasie des cryptes.
• Une augmentation du nombre de lymphocytes intra-épithéliaux (LIE) > 25 pour 100 cellules épithéliales.
• Une inflammation polymorphe du chorion (augmentation des lymphoplasmocytes).
L’augmentation des LIE est un signe histologique indispensable au diagnostic.
Les biopsies doivent être lues par un anatomopathologiste entraîné afin de ne pas méconnaître le diagnostic, ou à l’inverse de ne pas interpréter une mauvaise orientation des biopsies comme une atrophie villositaire. Des recoupes supplémentaires sur les blocs de paraffine doivent être demandées au moindre doute, et des marquages spécifiques (LIE, HLA-DR) doivent être proposés.
Difficultés diagnostiques
(8) Le déficit en IgA isolé est le plus fréquent des déficits immunitaires primitifs. La prévalence est estimée à 1/600 en Europe. Il est défini comme un taux d’IgA totales inférieur à 0,07 g/L avec des taux d’IgG et d’IgM normaux. Il est généralement asymptomatique, mais pourrait être associé à une fréquence accrue d’infections ORL, gastro-intestinales et bronchopulmonaires. Il faut noter que les normes des IgA totales varient en fonction de l’âge : la concentration en IgA sériques est très faible à la naissance et augmente durant l’enfance.
(9) En cas de déficit en IgA, les sérologies IgA ne sont pas interprétables, et des sérologies de type IgG doivent être réalisées : IgG anti-TG2, IgG anti-EM ou IgG antipeptides déamidés de la gliadine (anti-DGP). À noter qu’en France le dosage des IgA et IgG anti-DGP n’est pas remboursé.
(10) Dans les cas où le diagnostic de maladie coeliaque est infirmé après la FOGD, il faut savoir évoquer les diagnostics différentiels, qui sont principalement en cas de diarrhée et de douleurs abdominales chez l’enfant : les troubles fonctionnels intestinaux, une gastro-entérite infectieuse, une parasitose digestive, la maladie de Crohn ou plus rarement une entéropathie auto-immune. Les explorations complémentaires seront donc, en règle générale, poursuivies par le pédiatre gastroentérologue sollicité.
Lorsqu’un patient présente des symptômes liés à l’ingestion de gluten mais avec des sérologies coeliaques négatives sans déficit en IgA (et sous régime normal), la conduite à tenir dépend de la situation :
• en cas de forte suspicion clinique, un dosage des IgA anti-EM et une prise en charge par un pédiatre gastro-entérologue sont malgré tout à discuter, cf. (5) ;
• en cas de faible suspicion clinique, un contrôle des IgA anti-TG2 à 2 mois est malgré tout licite, en réintroduisant au préalable un régime normal si le gluten a été exclu par excès ;
• enfin, une hypersensibilité au gluten peut être évoquée. Cette pathologie de description récente est encore mal connue et reste un diagnostic d’élimination. Le diagnostic d’hypersensibilité au gluten peut être envisagé devant un patient présentant des symptômes liés à l’ingestion de gluten, avec des examens complémentaires tous normaux (en particulier IgA anti-TG2 et anti-EM négatives sous régime normal). Il est légitime d’adresser les patients chez lesquels ce diagnostic est évoqué auprès d’un gastroentérologue pédiatre afin de confirmer ou non cette suspicion diagnostique, demander si nécessaire des examens complémentaires pour éliminer d’autres diagnostics, et débuter un suivi.
Dépistage de la maladie coeliaque chez un enfant à risque asymptomatique : démarche diagnostique (PAP 2)
(1) Populations à risque
Le dépistage de la maladie coeliaque n’est pas recommandé dans la population générale. Il doit en revanche être systématique chez les sujets présentant un risque élevé de maladie coeliaque (risque estimé entre 2 et 10 % en fonction de la catégorie de patients). Ces individus « à risque » sont ceux ayant :
• un antécédent familial au premier degré de maladie coeliaque (parents, fratrie) ;
• une autre maladie auto-immune (en particulier diabète de type I, thyroïdite ou hépatite auto-immune) ;
• un déficit en IgA ;
• une anomalie génétique comme la trisomie 21, le syndrome de Turner ou le syndrome de Williams-Beuren.
(2) C’est le dosage des IgA anti-transglutaminase (anti-TG2) qui est actuellement la sérologie de référence, recommandée en première intention pour le diagnostic de la maladie coeliaque. Ce dosage doit toujours être associé à un dosage des IgA totales pour écarter un déficit en IgA (qui touche environ 5 % des patients coeliaques, le plus souvent sans expression clinique).
(3) Place du génotypage HLA classe II : le principal facteur de risque génétique de la maladie coeliaque est la présence d’un haplotype HLA classe II DQ2 et/ou DQ8 (cf. encart à la fin pour aller plus loin). Leur absence permet quasiment avec certitude d’éliminer une maladie coeliaque. Ces haplotypes sont cependant présents chez environ un tiers de la population générale, leur présence étant donc une condition nécessaire mais non suffisante pour le développement d’une maladie coeliaque. Les indications de la réalisation d’un génotypage HLA classe II sont bien moindres depuis les nouvelles recommandations diagnostiques de l’ESPGHAN. Sa réalisation n’est plus indispensable pour affirmer le diagnostic de maladie coeliaque sans biopsie, et il n’est plus recommandé en première intention dans les situations de dépistage dans certaines populations à risque comme les diabétiques de type I (la prévalence de l’haplotype HLA DQ2 et/ou DQ8 étant de presque 90 % chez les sujets diabétiques, il est recommandé de faire d’emblée les tests sérologiques). En revanche, il garde une place dans les situations de dépistage familial afin de déterminer si les parents au premier degré d’un patient coeliaque doivent être dépistés régulièrement (pas de dépistage nécessaire si génotype HLA non DQ2/DQ8). À noter que le génotypage HLA classe II n’est pas remboursé à l’heure actuelle, information devant être fournie aux familles lors de la prescription de cet examen. La réalisation de cet examen nécessite également la signature d’une attestation de consultation et d’un consentement par la famille. Nous suggérons donc dans cet algorithme de proposer le génotypage HLA aux patients afin de leur permettre de choisir s’ils souhaitent ou non le réaliser en fonction des arguments présentés ci-dessus (intérêt, coût, etc.).
(4) Les IgA antiendomysium (anti-EM) ne doivent être dosées qu’en seconde intention, uniquement selon les indications mentionnées dans l’algorithme diagnostique. Leur résultat est donné en inverse de dilution. Dans la situation d’un patient asymptomatique qui présente un résultat de dosage des anticorps anti-TG2 supérieur à 10 fois la normale (> 10N), il faut compléter le bilan par un dosage des anticorps antiendomysium (EM) sur un deuxième prélèvement.
(5) Les dernières recommandations européennes proposent, même dans le cas des patients asymptomatiques, qu’un diagnostic de certitude de maladie coeliaque puisse être fait sans confirmation histologique, lorsqu’il s’agit d’un individu appartenant à une population à risque, ayant à la fois des IgA anti-TG2 > 10N et des IgA anti-EM positives. Cependant, il est recommandé d’adresser ces patients en milieu gastroentérologique pédiatrique spécialisé devant de tels résultats, afin que tous les éléments soient bien pris en compte avant d’annoncer ce diagnostic « à vie » aux familles.
(6) Lorsque les conditions clinico-biologiques ne sont pas suffisantes pour affirmer le diagnostic de maladie coeliaque sans biopsie (IgA anti-TG2 positives mais < 10N, ou > 10N avec IgA anti-EM négatives), une endoscopie digestive haute doit être réalisée, avec réalisation de biopsies duodénales multiples. Les recommandations actuelles sont de prélever des biopsies multiples, au minimum 4 biopsies duodénales (idéalement 6), dont au moins 1 dans le bulbe, en raison de l’hétérogénéité des lésions.
(7) La maladie coeliaque se caractérise par l’association de 4 types de lésions histologiques, très caractéristiques de cette pathologie lorsqu’ils sont associés :
• Une atrophie villositaire de degré variable : elle peut être partielle, subtotale ou totale (classification de Marsh III A, B ou C)..
• Une hyperplasie des cryptes.
• Une augmentation du nombre de lymphocytes intra-épithéliaux (LIE) > 25 pour 100 cellules épithéliales.
• Une inflammation polymorphe du chorion (augmentation des lymphoplasmocytes).
L’augmentation des LIE est un signe histologique indispensable au diagnostic.
Les biopsies doivent être lues par un anatomopathologiste entraîné afin de ne pas méconnaître le diagnostic, ou à l’inverse de ne pas interpréter une mauvaise orientation des biopsies comme une atrophie villositaire. Des recoupes supplémentaires sur les blocs de paraffine doivent être redemandées au moindre doute, et des marquages spécifiques (LIE, HLA DR) doivent être proposés.
Difficultés diagnostiques
(8) Le déficit en IgA isolé est le plus fréquent des déficits immunitaires primitifs. La prévalence est estimée à 1/600 en Europe. Il est défini comme un taux d’IgA totales inférieur à 0,07 g/L avec des taux d’IgG et d’IgM normaux. Il est généralement asymptomatique, mais pourrait être associé à une fréquence accrue d’infections ORL, gastro-intestinales et bronchopulmonaires. Il faut noter que les normes des IgA totales varient en fonction de l’âge : la concentration en IgA sériques est très faible à la naissance et augmente durant l’enfance.
(9) En cas de déficit en IgA, les sérologies IgA ne sont pas interprétables, et des sérologies de type IgG doivent être réalisées : IgG anti-TG2, IgG anti-EM ou IgG anti-peptides déamidés de la gliadine (anti-DGP). À noter qu’en France le dosage des IgA et IgG anti-DGP n’est pas remboursé.
(10) En cas de sérologies négatives chez un patient appartenant à une population à risque et ayant un génotypage HLA DQ2 et/ou DQ8, le dosage des IgA anti-TG2 doit être renouvelé tous les 3 à 5 ans en cas d’antécédent familial de maladie coeliaque, et plus fréquemment (proposition de dépistage annuel) en cas de diabète de type I, d’autres maladies auto-immunes ou de pathologie génétique à risque.
(11) Chez un sujet asymptomatique appartenant à une population à risque, l’association d’IgA anti-TG2 positives à une augmentation isolée des lymphocytes intra-épithéliaux (sans atrophie villositaire) établit le diagnostic de maladie coeliaque latente. Dans ce cas, le patient peut être laissé au régime normal mais doit être surveillé régulièrement. En fonction de l’évolution du taux des anticorps, des réévaluations endoscopiques sont ensuite souhaitables afin de rechercher l’évolution vers une maladie coeliaque silencieuse ou symptomatique (développement d’une atrophie villositaire +/- associée à des signes cliniques).
(12) En cas de biopsies normales, les IgA anti-TG2 (ou IgG en cas de déficit) sont à contrôler tous les ans s’ils sont positifs, ou tous les 3 à 5 ans s’ils sont négatifs puisque l’on parle de sujets à risque. La réalisation d’un contrôle de l’endoscopie digestive haute sera décidée en fonction de l’évolution du taux des anticorps : s’ils restent élevés, un contrôle à 1 an paraît souhaitable.
Conclusion
La maladie coeliaque peut se présenter sous sa forme clinique typique, mais également sous forme de symptômes plus frustes qui doivent faire évoquer ce diagnostic ; et dans la majorité des cas, la maladie coeliaque est asymptomatique, et le diagnostic est fait dans un contexte de dépistage au sein de populations à risque. Ces dernières années, les indications de l’endoscopie digestive haute avec biopsies duodénales ont diminué, certaines situations clinico-biologiques permettant de réaliser un diagnostic sans nécessité de confirmation histologique. Cependant, le raisonnement doit être rigoureux afin de ne pas méconnaître une maladie coeliaque d’une part, et de ne pas poser de diagnostic par excès d’autre part.
Une fois le diagnostic confirmé, un régime sans gluten à vie doit être instauré, accompagné d’un suivi clinico-biologique régulier.
Prédisposition génétique : pour aller plus loin
Le HLA (Human Leukocyte Antigen) est le complexe majeur d’histocompatibilité (CMH) chez l’homme. Le HLA-DQ est un récepteur de surface des cellules présentatrices d’antigènes. Il s’agit d’un hétérodimère (chaîne alpha et bêta) de type CMH de classe II. La chaîne alpha DQ est codée par le gène HLA-DQA1 et la chaîne bêta est codée par le gène HLA-DQB1. Les différents sérotypes de HLA-DQ correspondent essentiellement à la chaîne DQB1. Un sérotype peut correspondre à plusieurs allèles. La table ci-dessous donne la correspondance entre le génotype et le sérotype pour les allèles à risque. Les sérotypes DQ2 à risque de maladie coeliaque correspondent aux haplotypes DQ2.5 (essentiellement) et DQ2.2, l’haplotype DQ2.3 n’étant pas à risque.
Il existe un effet « dose » pour le risque d’évolution vers la maladie coeliaque, avec par exemple un risque de 14,3 % en cas de DQ2 + DQ8, 10 % en cas de DQ2 + DQ2, 8,4 % en cas de DQ8 + DQ8, 2,9 % en cas de DQ2 + haplotype non à risque et 1,1 % en cas de DQ8 + haplotype non à risque. Les allèles DQB1*02 et DQA1*05 isolé donnent un faible risque de maladie coeliaque (0,05 % et 0,005 %). En l’absence d’allèle ou d’haplotype à risque, le risque de maladie coeliaque est inférieur à 0,04 %.
| Génétique | Sérotype | ||
|---|---|---|---|
| Allèles Sérotype HLA-DQA1 |
Allèles HLA-DQB1 |
Haplotype | |
| DQA1*05:01 DQA1*05:05 |
DQB1*02:01 DQB1*02:02 |
DQ2.5 | DQ2 |
| DQA1*03:01 DQA1*03:03 |
DQB1*03:02 | DQ8 | DQ8 |
| DQA1*02 | DQB1*02:01 DQB1*02:02 |
DQ2.2 | DQ2 |
| DQA1*05:01 DQA1*05:05 |
DQB1*03:01 | DQ7.5 | DQ7 |
Liens d’intérêts
Les auteurs déclarent ne pas avoir de liens d’intérêts.
Cet article fait partie du supplément Pas à Pas 2022 réalisé avec le soutien institutionnel de Procter & Gamble et Sanofi.


Références
Rawla P, Killeen RB, Joseph N. IgA Deficiency. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2022..
Husby S, Koletzko S, Korponay-Szabó I, Kurppa K, Mearin ML, Ribes-Koninckx C, et al. European society paediatric gastroenterology, hepatology and nutrition guidelines for diagnosing coeliac disease 2020. J Pediatr Gastroenterol Nutr. 2020;70(1):141‑56. DOI:10.1097/MPG.0000000000002497..
Fasano A. Clinical presentation of celiac disease in the pediatric population. Gastroenterology 2005;128:S68‑73..
Taylor AK, Lebwohl B, Snyder CL, Green PHR. Celiac disease. In: Adam MP, Ardinger HH, Pagon RA, Wallace SE, Bean LJH, Gripp KW, et al., editors. GeneReviews® [Internet]. Seattle (WA): University of Washington; 1993‑2022. PMID: 20301720..
Núñez C, Garrote JA, Arranz E, Bilbao JR, Fernández Bañares F, Jiménez J, et al. Recommendations to report and interpret HLA genetic findings in coeliac disease. Rev Esp Enferm Dig 2018;110(7):458‑461. DOI: 10.17235/reed.2018.5269/2017. PMID: 29722267.