Vous êtes ici
Thématique:
Traitement du paludisme d’importation de l’enfant
P. Minodiera , P. Imbertb
aUrgences enfants, CHU Nord, Chemin des Bourrely, 13015 Marseille bCentre de vaccinations internationales, hôpital d’instruction des armées Bégin, 69 avenue de Paris, 94160 Saint-Mandé Correspondance - Adresse e-mail : philippe.minodier@ap-hm.fr (P. Minodier).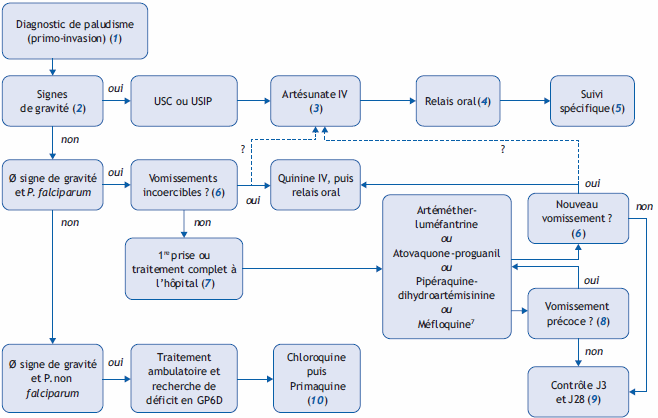
| Abréviations | |
|
USC : USIP : |
Unité de soins continus Unité de soins intensifs pédiatriques |
Arbre diagnostique – Commentaires
(1) Le diagnostic doit être évoqué sans délai devant un enfant fébrile de retour d’une zone d’endémie, quels que soit les signes cliniques associés ou la prévention effectuée. L’accès survient habituellement dans les 3 mois qui suivent le retour. Le diagnostic repose sur le frottis sanguin et la goutte épaisse. Les tests de diagnostic rapide ont une meilleure sensibilité pour P. falciparum que pour les autres espèces. Ils restent positifs au décours d’un accès traité.
(2) Les signes de gravité, proposés par l’OMS en 2000, sont cliniques (troubles neurologiques, défaillance respiratoire ou cardio-circulatoire, ictère, hémorragies, hémoglobinurie macroscopique) ou biologiques (anémie grave, hypoglycémie, acidose, hyperlactatémie, insuffisance rénale, hyperparasité- mie > 4 %). Une hyperparasitémie de 4 à 10 % sans autre critère de gravité ne justifie pas un traitement par artésunate.
(3) L’artésunate intraveineux a supplanté la quinine dans le trai- tement des accès graves. Il est mal évalué chez les nourrissons < 18 mois. Il est délivré sous ATU nominative. La dose est de 2,4 mg/kg (3 mg/kg si < 20 kg) à H0, H12, H24 puis toutes les 24 heures. Le traitement doit être réalisé en USC ou USIP. Si le paludisme a été contracté en Thaïlande ou au Cambodge, une bithérapie IV arté- sunate + quinine est indiquée. L’artésunate est aussi recommandé dans les rares formes graves dues aux Plasmodium non falciparum.
(4) Un relais est pris après 3 doses minimum d’artésunate par l’un des antipaludiques oraux recommandés, dès que la voie orale est possible.
(5) L’utilisation d’artésunate obéit à un protocole thérapeutique d’utilisation qui impose un suivi jusqu’à J28, notamment en raison d’anémies de survenue différée (examen et bilan san- guin à J3, J7, J14, J21 et J28).
(6) Des vomissements incoercibles justifient un traitement injectable. En l’absence d’AMM de l’artésunate dans cette indi- cation, la recommandation est la quinine IV (surveillance en USC ou USIP).
(7) Ces quatre traitements sont possibles en France, mais l’OMS recommande une thérapie combinée avec un dérivé de l’artémisinine (artéméther-luméfantrine ou pipéraquine-dihydroartémisinine). Le nombre total de prises orales peut être un frein chez le petit enfant. En raison du risque d’évolution vers un accès grave, des difficultés de prises orales et de la nécessité d’un suivi rapproché, le traitement est recommandé en hospitalisation, au moins pour les premières prises. Pour choisir le traitement, il faut également évaluer le risque de résistance de P. falciparum, qui peut être élevé dans certaines zones des Cambodge, Laos, Myanmar, Thaïlande et Vietnam, y compris avec l’artémisinine. De plus, quelle que soit la zone, la molécule prise en prophylaxie (méfloquine ou atovaquone-proguanil) ne devra pas être choisie en curatif.
(8) Toutes les molécules utilisées peuvent favoriser des vomisse- ments précoces. S’ils surviennent dans l’heure qui suit la prise (la demi-heure pour pipéraquine-dihydroartémisinine), elle doit être redonnée.
(9) Le suivi d’un paludisme à P. falciparum nécessite un contrôle parasitaire 72 heures après le début du traitement afin de vérifier que la parasitémie chute. Si ce n’est pas le cas, une autre molécule doit être donnée. L’enfant doit également être revu à J28.
(10) Les paludismes dus un Plasmodium non falciparum peuvent être traités par chloroquine, s’il n’y a ni signe de gravité, ni risque de résistance (Nouvelle-Guinée et certaines zones d’In- donésie). Le traitement est de 3 jours en ambulatoire, sans contrôle biologique. Afin d’éviter une rechute (formes hépa- tiques quiescentes), une éradication par primaquine doit être pratiqué dès le 1 er accès à P. vivax ou P. ovale. La dose est adaptée en cas de déficit en G6PD (risque d’hémolyse).
Liens d’intérêts
P. Minodier : conférences invitation en qualité d’intervenant(GSK) ; en qualité d’auditeur (Sanofi-Pasteur-MSD, Pfizer).
P. Imbert : l’auteur n’a pas transmis ses liens d’intérêts.


Références
Haut Conseil de la Santé Publique. Place de l’artésunate injectable dans le traitement du paludisme grave de l’adulte et de l’enfant. Disponible à : http://www.hcsp.fr/Explore.cgi/avisrapportsdomaine?clefr=311.
Imbert P, Minodier P. Paludisme de l’enfant. EMC (Elsevier Masson SAS, Paris), Maladies infectieuses,8-507-A-30,2011. Société de pathologie infectieuse de langue française. Prise en charge et prévention du paludisme d’importation à Plasmodium falciparum. Révision 2007 de la conférence de consensus de 1999 (texte long). Med Mal Infect 2008;38:68-117.
World Health Organization. Guideline for the treatment of malaria 2015. Disponible : http://apps.who.int/iris/bitstream/10665/162441/1/9789241549127_eng.pdf?ua=1&ua=1.