Vous êtes ici
Thématique:
Élévation des enzymes musculaires chez l’enfant
![]()
J. Durigneux1, C. Gitiaux2, P. de Lonlay3
1Centre de référence des maladies neuromusculaires AOC, neuropédiatrie et neurochirurgie de l’enfant, CHU Angers, Angers, France 2Service de neuropédiatrie, Hôpital Necker, AP-HP, Paris, France 3Centre de référence des maladies héréditaires du métabolisme, Hôpital Necker, AP-HP, université Paris-Cité, filière G2M, MetabERN, institut Necker-Enfants malades, INSERM, Paris, France Auteur correspondant - Adresse e-mail : pdelonlay@gmail.com (P. de Lonlay). Cliquez sur l'image pour l'agrandir.| Article validé par : | |
|
Société Française pour l’étude des Erreurs Innées du Métabolisme (SFEIM) Société Française de Neurologie Pédiatrique (SFNP) Groupe Francophone de Réanimation et d’Urgences Pédiatriques (GFRUP) |
|
Introduction
La rhabdomyolyse (RM) aiguë est une urgence parfois vitale, caractérisée par la destruction aiguë des myofibres squelettiques en réponse à un facteur déclenchant, le plus souvent un traumatisme, un effort physique, un médicament, un agent infectieux ou encore un jeûne inopiné. Elle peut être récurrente, faisant alors suspecter une maladie génétique. La destruction des cellules musculaires squelettiques induit une augmentation du taux sérique de créatine phosphokinase (CPK) supérieure à 1 000 UI/L (N < 250 UI/L) et la libération du contenu des myofibres dans la circulation sanguine, pouvant être responsable d’une insuffisance rénale aiguë (nécrose tubulaire) et d’une arythmie cardiaque. La présence d’une myoglobi nurie (urines de couleur brun/rouge, couleur du thé) indique que la RM est sévère, avec une élévation des CPK supérieure à 15 000 UI/L. Le taux de mortalité peut alors avoisiner les 10 % dans certaines cohortes, et être encore significativement plus élevé lorsque la rhabdomyolyse se complique d’insuffisance rénale. Quelle qu’en soit la cause, le déficit en ATP dans la cellule musculaire entraîne une augmentation du calcium intracellulaire par anomalie des pompes Na/K-ATPase et Ca2 + ATPase, et ainsi une nécrose secondaire des fibres musculaires.
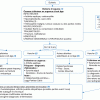
Orientation diagnostique devant une élévation des enzymes musculaires chez l’enfant
(1) La RM se présente classiquement par des myalgies, parfois des douleurs diffuses mal définies, une incapacité à se mettre debout. De façon plus rare, il peut s’agir d’un enfant prostré, d’un malaise sévère, d’un tableau de choc hypo volémique ou d’un coma. La présence d’urines foncées (en faveur d’une myoglobinurie) permet de l’évoquer rapidement. Les diagnostics différentiels sont les affections ostéoarticulaires, un syndrome de Guillain-Barré, une myélite, une myasthénie (fatigabilité musculaire).
Sur le plan biologique, devant toute cytolyse hépatique (cf. note Thierry Lamireau), il est indispensable de doser les CPK.
Le bilan paraclinique initial comprend : dosage des CPK (RM confirmée si > 1 000 UI/L), ionogramme sanguin, calcémie, phosphatémie, urée, créatinine, bilan étiologique en cas d’orientation particulière à l’interrogatoire, ECG à la recherche d’une complication.
(2) Certaines situations constituent une urgence : choc hypovolémique, coma, insuffisance rénale aiguë (anurie), arythmie. Une RM avec CPK > 15 000 UI/L est toujours une urgence, notamment chez un patient non suivi, car on ne sait pas quelle sera l’intensité de la crise de RM dans les heures qui suivront. Il faut alors hospitaliser le patient en réanimation. Les patients connus atteints d’une maladie génétique responsable de RM doivent être pris en charge en urgence en cas de douleurs musculaires, même si le taux de CPK de départ est normal. Cette prise en charge consistera en une surveillance cardiaque en continu, une hyperhydratation (3 L/m2/j avec une perfusion sans potassium dès que CPK > 6 000 UI/L), l’arrêt des médicaments potentiellement responsable de RM, l’arrêt des médicaments hyperkaliémiants (IEC, spironolactone), un bilan biologique toutes les 6 heures (glycémie, ionogramme notamment la kaliémie (risque d’hyperkaliémie, mais aussi d’hypokaliémie du fait d’une perfusion sans potassium), urée, créatinine, CPK). Des protocoles d’urgence sont disponibles sur le site internet de la filière G2M (www.filiere-g2m.fr/) à l’onglet « urgences » : pour un premier épisode (patient non connu), pour un patient connu qui a fait une RM sévère, pour un patient connu qui a fait une RM peu sévère, pour le déficit en RYR1, pour le déficit en lipin-1 et pour le déficit en TANGO2.
(3) La surveillance biologique régulière (CPK toutes les semaines jusqu’à normalisation) est un élément clé de la prise en charge, notamment pour l’enquête étiologique.
En cas de premier épisode non sévère et résolutif (CPK normalisées à 1 mois), on évoquera en premier lieu les causes extrinsèques de RM, de loin les plus fréquentes : cf. paragraphe 4. Cependant, des causes traitables dépistables par un bilan biochimique (hypothyroïdie, déficit de l’oxydation des acides gras) doivent être recherchées de façon large.
En cas de RM récidivantes et/ou très sévères (CPK > 50 000 UI/L à titre indicatif, sans qu’il y ait de curseur précis concernant le seuil de CPK dans la littérature), des causes métaboliques et calciques doivent être évoquées : cf. paragraphe 5.
En l’absence de normalisation des CPK, l’enquête doit s’orienter vers des étiologies neuromusculaires (y compris les myo pathies métaboliques type maladie de Mc Ardle) et inflammatoires : cf. paragraphe 6.
(4) Étiologies extrinsèques de RM : formes résolutives non récidivantes
Un traumatisme (compression mécanique, brûlure, électrisation), un effort physique d’intensité inhabituelle, certains médicaments (propofol, halogénés, neuroleptiques, AINS, méthylphénidate, statines…) ou certains agents infectieux (par exemple : grippe, Covid-19, mycoplasme…) sont des causes fréquentes de RM. L’interrogatoire suffit le plus souvent pour les identifier.
Cependant, ces facteurs peuvent aussi décompenser une maladie génétique sous-jacente. La difficulté est de reconnaître une cause génétique sous-jacente, qui rendra compte de la récurrence des accès.
(5) Les principales causes génétiques à évoquer devant des accès récurrents de RM sont :
(5a) Chez le jeune enfant (avant 6 ans) : causes métaboliques, de transmission récessive autosomique, avec normalisation des CPK
En cas de signes associés :
• les déficits de l’oxydation des acides gras (DOAG) : hypoglycémie, hyperammoniémie et/ou atteinte myocardique/trouble du rythme cardiaque, voire syndrome de Reye (insuffisance hépato cellulaire, hyperammoniémie et coma) ;
• autres anomalies du glycogène et de la glycolyse : hyperuricémie, anémie hémolytique ;
• plus rarement d’autres maladies métaboliques :
- déficit en TANGO2 : retard mental, dystonie, atteinte hépatique, hypothyroïdie et atteintes cardiaques (QT long, Brugada…),
- trouble de la glycosylation (CDG) : retard de croissance, anomalies hépatiques, cardiomyopathie dilatée, hypo glycémie transitoire,
- maladies mitochondriales : hyperlactatémie.
En cas de RM isolée :
• déficits en lipin-1 (qui donnent des RM sévères avant 6 ans) : CPK > 50 000 UI/L ;
• DOAG
(5b) Chez l’adolescent, jeune adulte :
En cas de signes associés : causes métaboliques, de transmission récessive autosomique, avec normalisation des CPK :
• DOAG ;
• plus rarement d’autres maladies métaboliques :
- déficit en TANGO2
- maladies mitochondriales
En cas de RM isolée :
• causes métaboliques, de transmission récessive autosomique, avec normalisation des CPK :
- déficits en lipin-1,
- DOAG
• causes calciques, avec normalisation des CPK ou élévation chronique des CPK :
- mutations dans le gène RYR1 de transmission dominante autosomique ou autres gènes apparentés (CACNA1S par exemple) : une anesthésie générale ou un effort physique peuvent être un facteur déclenchant, et la RM peut s’accompagner d’une hyperthermie maligne.
(6) Les principales causes génétiques à évoquer devant une RM chronique (CPK élevées en permanence) sont :
• canalopathies musculaires : maladies des canaux ioniques musculaires (myotonies et paralysies périodiques familiales) : crampes nocturnes, accès de paralysies musculaires et modifications du taux de potassium (hypo/hyperkaliémie) au réveil ou à distance d’un effort ;
• glycogénoses musculaires et anomalies de la glycolyse :
- glycogénose de type V (Mc Ardle) : notion de second souffle (possibilité de reprendre une activité physique après un temps de pause), déficit musculaire. Accès de RM, sans normalisation des CPK entre les accès,
- maladie de Pompe (glycogénose type II) : déficit musculaire, cardiomyopathie hypertrophique (espace PR court à l’ECG), insuffisance respiratoire ;
• causes neuromusculaires :
- dystrophinopathies (dystrophie musculaire de Duchenne/Becker, transmettrices DMD/B) : déficit musculaire, hypertrophie des mollets, parfois retard cognitif,
- Dystrophies musculaires des ceintures (LGMD pour Limb Girdle Muscular Dystrophy) : déficit musculaire,
- myopathies congénitales notamment en lien avec le gène RYR1 : déficit musculaire ;
• myosites dans le cadre de pathologies inflammatoires : syndrome inflammatoire et/ou atteinte cutanée (dermatomyosite).
La présentation clinique et biologique aide au diagnostic étiologique, une maladie génétique devant être recherchée si la RM est sévère ou récurrente quel que soit le facteur déclenchant.
Toute RM sévère (> 15 000 UI/L) ou récidivante (dès le 2e épisode quelle que soit la valeur de CPK) ou RM chronique nécessite un avis spécialisé auprès d’un médecin spécialiste en maladies métaboliques et/ou neuropédiatre spécialisé en maladies neuromusculaires, au mieux dans le cadre d’un centre de compétence ou de référence.
(7) Bilan diagnostique
En urgence, à réaliser en phase aiguë, en parallèle de la prise en charge thérapeutique : seuls les DOAG et les causes inflammatoires peuvent être diagnostiqués rapidement en phase aiguë. L’interrogatoire rétrospectif peut orienter pour les autres causes. Dans le sang, outre le dosage des CPK et la surveillance hydro-électrolytique, le bilan comporte : une NFS avec recherche d’anémie hémolytique (déficit de la glycolyse), un bilan inflammatoire, des anticorps antimyosite (cause inflammatoire), la glycémie (DOAG, glycogénoses, CDG), la kaliémie, un profil des acylcarnitines et un dosage de la carnitine, une ammoniémie (DOAG), un point redox (DOAG, maladie mitochondriale). Dans les urines : une chromatographie des acides organiques urinaires (DOAG, maladie mitochondriale). Une biopsie de muscle avec marquages spécifiques est réalisée à la phase aiguë uniquement si une cause inflammatoire est suspectée, pour discuter d’une corticothérapie à forte dose dans le cadre d’une dermatomyosite (avis spécialisé).
Sans urgence, au décours de la RM et en l’absence d’orientation diagnostique particulière : examen clinique et dosage des CPK toutes les semaines. Si l’examen clinique est normal et les CPK se sont normalisées avant 1 mois, le bilan de 1re intention doit être réalisé de façon large si non fait initialement (TSH, profil Acylcarnitines, dosage carnitine, lactates, point redox, CAOu, bilan inammatoire), et proposition de panel de gènes impliqués dans le métabolisme incluant les gènes calciques, de façon systématique même en cas de premier épisode (en lien avec un centre spécialisé). Il y a en effet un bénéfice à diagnostiquer une mutation dans le gène RYR1 par exemple, avec une prévention des RM notamment au moment d’anesthésies générales, et la possibilité d’un traitement. Une biopsie musculaire (+/– ENMG) sera discutée en seconde intention pour histologie, avec recherche d’une dystrophie musculaire, étude systématique des protéines membranaires en western blot, recherche d’une surcharge en lipides (non pathognomonique d’un DOAG) ou en glycogène, immunohistochimie de la myophosphorylase pour une maladie de Mc Ardle. Si une biopsie musculaire est réalisée, des myoblastes pourront être conservés (selon les possibilités locales), ainsi qu’un fragment de muscle, dans l’azote liquide ou à –80 °C. Discuter la réalisation d’une épreuve d’effort ou un grip test à la recherche d’éléments en faveur d’une maladie de Mc Ardle. Un ENMG sera discuté en cas de suspicion de maladie des canaux ioniques musculaires.
En l’absence de normalisation des CPK à un mois, un avis spécialisé de centre de compétence ou de référence neuromusculaire doit être demandé, avec éventuellement la réalisation d’une biopsie musculaire à prévoir, notamment en l’absence d’orientation clinique. En fonction des résultats de la biopsie et de l’orientation clinique, des analyses génétiques ciblées ou plus larges pourront être réalisées.
Conclusion
La rhabdomyolyse est une urgence avec un potentiel risque vital. Le contrôle des CPK permet de s’assurer de l’absence de rhabdo myolyse chronique orientant vers des pathologies spécifiques. Un facteur déclenchant peut être à l’origine de la décompensation d’une cause génétique, et le bilan biologique initial doit donc comporter la recherche d’une pathologie métabolique, et facilement une étude de panel de gènes.
Liens d’intérêts
Les auteurs déclarent ne pas avoir de liens d’intérêts.
Cet article fait partie du supplément Pas à Pas 2023 réalisé avec le soutien institutionnel de Procter & Gamble et Sanofi.


Références
Cervellin G, Comelli I, Lippi G. Rhabdomyolysis: historical background, clinical, diagnostic and therapeutic features. Clin Chem Lab Med 2010;48(6):749-56.
Berardo A, DiMauro S, Hirano M. A diagnostic algorithm for metabolic myopathies. Curr Neurol Neurosci Rep 2010;10(2): 118-26.
Scalco RS, Gardiner AR, Pitceathly RDS, Zanoteli E, Becker J, Holton JL, et al. Rhabdomyolysis: a genetic perspective. Orphanet J Rare Dis 2015;10:51.
Lundberg IE, Tjärnlund A, Bottai M, Werth VP, Pilkington C, Visser M, et al. 2017 European League against Rheumatism/American College of Rheumatology classification criteria for adult and juvenile idiopathic inflammatory myopathies and their major subgroups. Ann Rheum is 2017;76(12):1955-64.
Dlamini N, Voermans NC, Lillis S, Stewart K, Kamsteeg EJ, Dros G, et al. Mutations in RYR1 are a common cause of exertional myalgia and rhabdomyolysis. Neuromuscul Disord 2013;23(7): 540-8.